Câncer de Próstata é tema de artigo do Medicina Atual
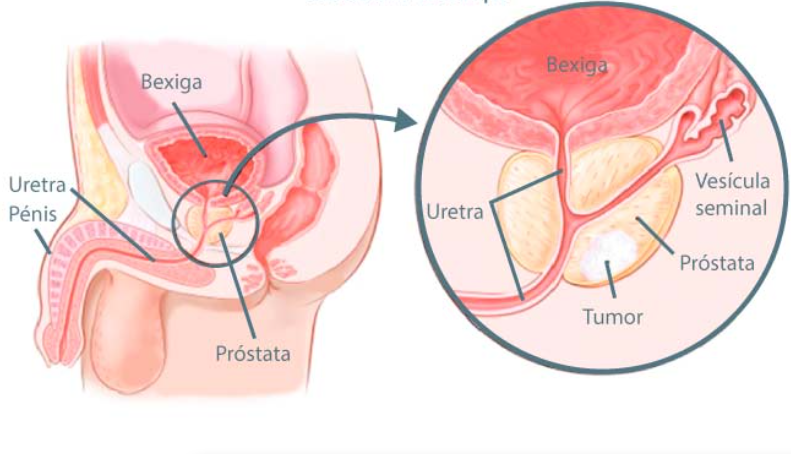
O Câncer de próstata é uma das doenças mais temidas pelo sexo masculino e os dados alertam: é preciso ter cuidado. Além de ser a quinta causa de morte no mundo, esse tipo de câncer é o segundo que mais afeta o sexo masculino.
De acordo com o Instituto Nacional do Câncer (INCA), em nível nacional, o câncer de próstata fica atrás apenas do câncer de pele não-melanoma, com cerca de 65 mil novos casos em 2020 e 16 mil mortes.
Por 75% dos casos no mundo ocorrerem a partir dos 65 anos, esse câncer é considerado um enfermidade da terceira idade. Em síntese, a incidência e mortalidade variam no mundo de acordo com a população estudada, a susceptibilidade genética e cuidados regionais de saúde.
Os únicos fatores de risco bem estabelecidos para a doença são a idade avançada, raça negra e história familiar.
A seguir, você vai saber:
Leia artigo
Quer saber mais sobre esse tipo de câncer? Então leia o artigo completo do portal Medicinal Atual. Escrito pelo urologista e doutor em Técnica Cirúrgica pela UFMG, Humberto Lopes, o texto aborda os principais sinais, sintomas, diagnóstico, tipos e muito mais.
Material super completo para os residentes que desejam seguir a especialidade de urologia. Conheça também o portal do Revisamed – Revisional em Medicina.
INTRODUÇÃO
O câncer de próstata é o segundo tumor mais diagnosticado no homem e é considerado a quinta causa de morte no mundo. No Brasil, o câncer de próstata é também o segundo mais comum entre os homens (atrás apenas do câncer de pele não-melanoma), com cerca de 65 mil novos casos em 2020 e 16 mil mortes, segundo o INCA.
Estima-se em todo mundo uma incidência de 2.3 milhões de novos casos e 740 mil mortes em 2040 em decorrência do crescimento e envelhecimento da população. Mais do que qualquer outro tipo, é considerado um câncer da terceira idade, já que cerca de 75% dos casos no mundo ocorrem a partir dos 65 anos.
A incidência e mortalidade variam no mundo de acordo com a população estudada, a susceptibilidade genética e cuidados regionais de saúde. Os únicos fatores de risco bem estabelecidos para a doença são a idade avançada, raça negra e história familiar.
Os homens com parentes em primeiro grau com diagnóstico de câncer próstata apresentam um risco duas vezes aumentado de serem acometidos, e se antecedentes de tumor com o pai e irmão ou dois irmãos o risco pode ser de cinco a sete vezes.
Cerca de 9% dos pacientes apresentam câncer de próstata hereditário, definido como três ou mais familiares acometidos ou dois parentes que desenvolveram a doença com menos de 55 anos de idade. Mutações genéticas têm sido identificadas entre homens com doença não hereditária, geralmente associada ao gene BRCA2, dentre outros.
Uma variedade de fatores ambientais e exógenos tem sido implicada ao risco de desenvolvimento ou progressão de câncer de próstata latente para tumor clinicamente significativo. Entretanto, não existem, no momento, intervenções farmacológicas ou na dieta que realmente sejam efetivas. Homens hipogonádicos apresentam risco abaixo da média de serem acometidos, enquanto a reposição de testosterona não aumenta o risco de câncer de próstata.
RASTREAMENTO
O rastreamento do câncer de próstata consiste em examinar, sistematicamente, homens assintomáticos (mas de risco), entre 45 e 70 anos, e é indicado por entidades de saúde pública com objetivo de reduzir a mortalidade e manter a qualidade de vida.
Entretanto, estudos recentes demonstraram que o rastreamento está associado com aumento de diagnóstico precoce, detecção de doença em estádio inicial (indolente) e menos doença avançada, mas não observando melhora na sobrevida dos pacientes diagnosticados e tratados após rastreio.
Assim, mesmo existindo controvérsias sobre rastreamento com PSA (Antígeno Prostático Específico) alguns estudos demonstram de maneira inequívoca que o diagnóstico precoce pode salvar vidas, com uma redução de 20 -25% de mortalidade por câncer de próstata.
A maioria das entidades urológicas internacionais recomenda a dosagem do PSA:
- como um teste basal, em homens aos 40 anos, quando poderá avaliar (prever) o risco de doença durante a vida;
- precocemente, em afrodescendentes e naqueles com antecedentes familiares de câncer de próstata;
- mesmo naqueles acima de 70 anos, também com risco de câncer de próstata, mas expectativa de vida superior a 10 anos.
Diferente do rastreamento, a possibilidade de detecção precoce da doença pode ser uma estratégia adaptada e individualizada, mas ainda associada com riscos de diagnósticos em excesso no grupo de pacientes de risco como citamos anteriormente.
É reconhecido que homens com PSA >1ng/ml aos 40 anos e > 2ng/ml aos 60 anos apresentam maior risco de metástases e morte pelo câncer durante a vida.
Assim, para aqueles pacientes que procuram para avaliação e diagnóstico precoce devem ser informados sobre a dosagem de PSA e realização do exame físico (toque retal), sobretudo naqueles maiores de 50 anos, ou com 45 anos e com antecedentes familiares, nos afrodescendentes e naqueles com 40 anos, mas portadores de mutações genéticas.
O toque digital da próstata na atenção primária não deve ser utilizado como único método, devido à baixa sensibilidade, especificidade e pela provável inexperiência do examinador em não poder excluir o câncer de próstata.
Recentemente, múltiplos testes e exames, além do PSA, têm sido adicionados à prática clínica a fim de evitar biópsias desnecessárias, incluindo PCA3, e outras calicreínas como as incorporadas ao PHI (Índice de Saúde Prostática) e ao 4Kscore.
A ressonância magnética multiparamétrica (RNM), utilizada principalmente no estadiamento, tem aumentado seu papel na avaliação inicial dos casos suspeitos e com potencial indicação de biópsia.
Mesmo utilizando métodos de imagens e testes, mas com objetivo de evitar biópsias desnecessárias e sobrediagnóstico, podemos utilizar outras ferramentas (calculadoras de risco) reconhecidas em diversos estudos: http://myprostatecancerrisk.com/
CONSIDERAÇÕES PRÁTICAS
1 – COMPARTILHAR COM PACIENTE SOBRE RASTREAMENTO E UTILIZAR O CONSENTIMENTO INFORMADO.
2 – REALIZAR A DOSAGEM DE PSA COMO RASTREIO APENAS EM HOMENS ENTRE 45-70 ANOS.
3 – DISCUTIR A FREQUÊNCIA DO RASTREIO E APÓS 60 ANOS APENAS SE PSA >1 ng/ml.
4 – EM PACIENTES COM PSA ≥ 3ng/ml, ORIENTAR PARA REPETIR EM 4-6 SEMANAS.
5 – AVALIAR TESTES SECUNDÁRIOS (PSA LIVRE, DENSIDADE), OUTROS MARCADORES E RNM ANTES DE BIOPSIAR.
6 – PACIENTES COM DOENÇA DE BAIXO RISCO DEVEM SER ORIENTADOS SOBRE A VIGILÂNCIA ATIVA E ENCAMINHADOS AO UROLOGISTA.
DIAGNÓSTICO
O câncer de próstata é usualmente suspeitado pelo exame físico e/ou valores do PSA, mas o diagnóstico definitivo depende do anatomopatológico da biópsia de próstata.
EXAME DIGITAL RETAL
A maioria dos cânceres de próstata está localizada na zona periférica da próstata (parte mais externa e acessível ao toque) e em 18% dos casos pode ser suspeitado ao toque independentemente dos níveis de PSA.
ANTÍGENO PROSTÁTICO ESPECÍFICO (PSA)
Mesmo não sendo câncer específico e estar elevado na hiperplasia prostática benigna, prostatite e outras condições não malignas, a utilização do PSA como marcador revolucionou o diagnóstico do câncer de próstata. É considerado melhor preditor de câncer do que o exame digital da próstata ou ultrassonografia transrretal.
Não existe um valor definido de PSA e risco câncer, mas valores maiores indicam maior possibilidade de doença e valores baixos podem ter risco conforme a tabela 1.
TABELA 1

RISCO DE CÂNCER DE PRÓSTATA EM RELAÇÃO A VALORES BAIXOS DE PSA
Uma avaliação individualizada do PSA em cada paciente é fundamental e pode quase sempre necessitar da utilização de alternativas do PSA na decisão clínica, principalmente naqueles cujo valor do PSA encontra-se entre 2,5 -10 ng/ml.
PSA livre / PSA total
Naqueles com valores da relação livre/total abaixo de 10, o risco de câncer na biópsia é 56%, e quando superior a 25 é de apenas 8%.
Densidade do PSA
Consiste na relação entre valor do PSA/volume da próstata (avaliada por ultrassonografia transrretal), quando este valor é superior a 15 prediz maior risco.
Velocidade do PSA
Um aumento anual absoluto de 20 % ou 0,5ng /ml impõe maior risco e deve ser considerado na decisão para indicar biópsia.
OUTROS TESTES
Em situações especiais, principalmente em pacientes já submetidos à biópsia de próstata e que continuam em risco e precisa tomada de decisão por parte do especialista, a realização de testes como PHI (Índice de Saúde Prostática), 4Kscore e PCA 3 (na urina pós-massagem prostática) podem ser métodos auxiliares para indicar ou não a biópsia.
RESSONÂNCIA MAGNÉTICA DA PRÓSTATA
Estudos recentes têm demonstrado papel importante da RNM na diminuição das indicações de biópsias, reduzindo diagnóstico de doença de baixo grau (indolentes) e mantendo ou melhorando a detecção de tumores significantes.
A interpretação e relatório do exame devem ser realizados por métodos padronizados e por radiologistas familiarizados com a técnica: PI-RADS- v2 (Próstata Imagina Repor Ting and. Data System).
Devem ser utilizadas, nos casos prioritários de risco para câncer e naqueles casos de RNM normal, as calculadoras de risco, a densidade de PSA e outros biomarcadores podem auxiliar em quais pacientes deve-se evitar a biópsia. Nos pacientes que apresentam RNM alterada a biópsia deve ser aleatória e também direcionada à área suspeita.
Ressalta-se que RNM não deve ser utilizada como rastreamento, mas sim de maneira criteriosa nos indivíduos que são candidatos a uma biópsia.
BIÓPSIA PROSTÁTICA
A decisão de indicar uma biópsia é baseada na suspeita do exame físico (exame digital), níveis de PSA (livre/total, densidade e velocidade) e métodos de imagem (RNM), considerando a idade, comorbidades e discutindo com o paciente as complicações e consequências terapêuticas do diagnóstico.
A biópsia é realizada com auxílio da ultrassonografia transrretal e, mais recentemente, em decorrência de menores taxas de infecção, a via transperineal tem sido proposta.
Usualmente, sob anestesia, é retirado cerca de 12 fragmentos e, em casos de re-biópsia, pode-se ultrapassar a 20 fragmentos (biópsia por saturação). Recomenda-se a antibioticoprofilaxia com quinolonas por 3 a 7 dias, associada à desinfecção retal com povidine.
Recentemente, na tentativa de melhorar a acurácia e detectar realmente os tumores significantes, tem sido, gradualmente, utilizada a biópsia por fusão. Consiste na realização das punções na próstata utilizando fusão da ultrassonografia à RNM de forma acoplada ou cognitiva.
Não é incomum a necessidade de repetir a biópsia (após primeira negativa) durante o acompanhamento do paciente e, geralmente, as principais indicações são:
– níveis de PSA elevados ou em elevação;
– exame físico suspeito – risco de câncer em 5% – 30%;
– achados na primeira biópsia de glândulas atípicas suspeitas (ASAP) – risco de câncer em 30%;
– achados na primeira biópsia de múltiplos focos de neoplasia intraepitelial (PIN) – risco de câncer em 30%;
– ressonância magnética suspeita (Pi-Rads ≥3).
Os resultados histológicos podem demonstrar ausência de tumor, casos incertos (merecem discussão intradepartamental ou consulta externa) e casos confirmados de adenocarcinoma da próstata. Cada fragmento deve ser relatado individualmente, incluindo tipo histológico. O grau de Gleason (GS), que é baseado nos aspectos arquiteturais de tumor, é classificado de 1 a 5 (grau dominante e o secundário) e fornece um excelente prognóstico clínico. Entretanto, com objetivo de facilitar comunicação dos patologistas com clínicos e pacientes, a Sociedade Internacional de Patologia Urológica (ISUP) adotou a classificação em cinco grupos: grau de ISUP 1 (GS 3 + 3), grau 2 (GS 3 + 4), grau 3 (GS 4 + 3), grau 4 (GS 4 + 4, 3 + 5, 5 + 3) e grau 5 (GS 9-10). (QUADRO 1)
A proporção e extensão dos fragmentos positivos correlacionam-se com o grau de ISUP, com o volume tumoral e com as margens cirúrgicas nos espécimes de prostatectomia radical e prediz recorrência bioquímica pós-tratamento cirúrgico e radioterapia.

ESTADIAMENTO
O estadiamento do câncer de próstata, após diagnóstico histológico, visa fornecer e conhecer a extensão local da doença, a presença ou não de linfonodos e metástases.
Além do exame físico e da ultrassonografia, a RNM tem papel importante no estadiamento local e planejamento terapêutico, entretanto, a experiência do interpretador do exame é fundamental. Com esta finalidade (estadiamento) deve ser realizada após 6 semanas da biópsia devido aos artefatos (sangramento pós-punção).
O estadiamento linfonodal pode ser realizado pela Tomografia Computadorizada e RNM, embora com sensibilidade inferior a 40%. A presença de linfonodos >8 mm na pelve e >10 mm fora da pelve pode ser considerada maligno.
Na avaliação óssea, a cintilografia permanece como método de escolha, embora sua sensibilidade seja dependente do valor do PSA e do grau de ISUP. Deve ser realizada em todos pacientes sintomáticos (independentemente do valor de PSA e ISUP), sendo positiva em 3 % dos pacientes com PSA < que 10 ng/ml, 5 % com PSA entre 10-20 ng/ml e 16 % dos pacientes com PSA entre 20-50 ng/ml.
Recentemente, o PET-TC PSMA (antígeno prostático específico de membrana) tem sido utilizado no estadiamento da doença de alto risco, além de ser essencial na avaliação das recidivas bioquímicas pós-tratamento, principalmente na avaliação de linfonodos e com reconhecido impacto na decisão clínica pelo urologista e oncologista clínico.
TRATAMENTO
O tratamento do câncer de próstata, assim como a decisão de rastreamento e diagnóstico, deve ser considerado em relação à idade do paciente, presença de comorbidades, condições clínicas e expectativa de vida. Uma expectativa de vida de 10 anos é comumente utilizada como limite para beneficiar-se do tratamento local da doença. Assim, um paciente com 70 anos ou mais que apresenta uma condição clínica fragilizada deve ser avaliado por um geriatra.
Além das considerações anteriores, o grau de ISUP e o estadiamento (classificação de risco – tabela 2) terão papel importante na decisão de realizar tratamento local ou uma conduta conservadora (vigilância ativa ou observação vigilante), diminuindo o sobre-tratamento em alguns indivíduos. (Tabela 3)

VIGILÂNCIA ATIVA X OBSERVAÇÃO VIGILANTE
A proposta da vigilância ativa é evitar tratamento desnecessário em homens com doença clinicamente localizada que não requer tratamento imediato, mas que, ao mesmo tempo, possa ser realizada naqueles quando necessitarem tratamento devido progressão da doença ou decisão do próprio paciente.
Estes pacientes permanecem em programas de reavaliações estruturadas periódicas com dosagem de PSA, exame físico, RNM e repetidas biópsias, e, assim, o tratamento curativo é determinado no momento que a doença apresentar potencial risco, mas ainda curável e sempre considerando a expectativa de vida.
Por outro lado, a conduta de observação vigilante refere-se ao tratamento conservador para pacientes não aptos para tratamento curativo no momento do diagnóstico, mas são observados em relação à progressão local ou sistêmica da doença e, oportunamente, tratados paliativamente de acordo com os sintomas e objetivando sempre manter a qualidade de vida.
PROSTATECTOMIA RADICAL
O objetivo da abordagem cirúrgica é a erradicação do câncer e, sempre que possível, manter resultados funcionais (continência, função erétil) e atingir bons resultados oncológicos, associando-se a uma baixa morbidade. O procedimento consiste em remover toda a próstata com sua cápsula intacta, as vesículas seminais, seguida de anastomose uretra-colo vesical e linfadenectomia pélvica nos pacientes de risco intermediário e alto.
A técnica pode ser realizada desde a via perineal e retropúbica (aberta) até laparoscópica e, mais recentemente, robótica assistida. Não há uma recomendação específica sobre a superioridade de uma técnica com a outra, mas os riscos de margens positivas e recuperação precoce da continência devem ser discutidos com o paciente, pois é sabidamente reconhecido o papel da experiência do cirurgião e número cirurgias no hospital onde o paciente será tratado.
RADIOTERAPIA
As inovações recentes da radioterapia como a intensidade modulada (IMRT) e com imagem guiada (IGRT) é reconhecida como a melhor opção, pois se adapta continuamente e automaticamente aos contornos do órgão alvo (próstata) e com menos toxicidade. O bloqueio hormonal neoadjuvante e adjuvante (6 meses ou 2-3 anos), associado à radioterapia em pacientes portadores de doença de risco intermediário e alto, têm comprovada superioridade em relação à radioterapia isolada.
BRAQUITERAPIA
Esta modalidade terapêutica consiste no implante permanente de sementes radioativas (Iodo -125 – mais comum, Palladium -103 ou Cesium-131) no interior da próstata. Apresentam melhores resultados nos pacientes estádio T1, ISUP 1 com menos 50% dos fragmentos envolvidos, PSA < 10 ng/ml e sintomas miccionais leves (IPSS < 12).
As novas tecnologias como Ultrassom Focal de Alta Intensidade (HIFU), a Crioterapia e a Terapia focal fotodinâmica têm sua utilização ainda investigacional, com resultados heterogêneos em longo prazo, sendo restritos a alguns centros.
FOLLOW-UP
Os pacientes devem ser monitorados regularmente, pois cerca de 5-20% mantêm com PSA detectável ou persistentemente elevado após prostatectomia radical (> 0.1 ng/ml após 4-8 semanas da cirurgia). Isto pode ser em decorrência de doença local persistente, metástase pré-existente ou tecido benigno residual. Por outro lado, cerca de 27-53 % de todos pacientes submetidos à prostatectomia ou radioterapia apresentam elevação do PSA (recorrência bioquímica) e poderão necessitar, em alguns casos, de re-estadiamento local e/ou sistêmico, seguido de tratamento local (adjuvante ou resgate) e /ou sistêmico.
CONSIDERAÇÕES FINAIS
Os pacientes que procuram o médico generalista e que desejam informações e cuidados a respeito do câncer de próstata devem ser informados sobre a idade e momento ideal para rastreamento, assim como as consequências da realização dos exames e dos possíveis tratamentos. Recomenda-se a dosagem do PSA a partir de 45 anos naqueles com antecedentes familiares de câncer de próstata e nos afrodescendentes, senão, a partir de 50 anos. Esta é orientação da maioria das Associações Urológicas, incluindo a SBU, que também recomenda a realização do exame físico (exame digital), o que melhora a sensibilidade na detecção precoce de cânceres significativos. Entretanto, a periodicidade deverá ser discutida com o paciente individualmente de acordo com valores de PSA. Sabe-se que valores de PSA < 1,0 ng/ml aos 50 anos e < 2 ng/ml aos 60 anos é preditivo de baixo risco de mortalidade por câncer de próstata.
Por outro lado, em pacientes que não apresentam riscos, com PSA de 3 ng/ml em uma avaliação esporádica, deve-se ter o exame repetido, pois alguns estudos demonstraram retorno do PSA à normalidade em 44 % dos casos, após 12 meses. Ressalta-se que na primeira avaliação pelo clínico, este deve solicitar apenas a dosagem do PSA total. Naqueles pacientes cujo PSA é superior a 2,5 ng/ml, já repetido, deve-se orientar a dosagem da fração livre do PSA (relação PSA livre/total – geralmente fornecida pelo laboratório). Valor abaixo de 15 % é indicativo para avaliação pelo especialista (Urologista).
O Urologista, além do exame físico, avalia a velocidade do PSA e a densidade do PSA, e uma discussão compartilhada com paciente decide sobre a necessidade ou não de biópsia prostática. Nos pacientes de risco, com real probabilidade de câncer, tem-se associado a RNM na avaliação inicial, pois esta poderá excluir cerca de 25% dos pacientes da biópsia.
Os pacientes com biópsia negativa devem continuar sob avaliação periódica, pois cerca de 10-15 % dos pacientes poderão necessitar de re-biópsia em decorrência da manutenção da suspeita ou de elevação do PSA durante o seguimento. Nestes casos, os novos marcadores têm papel essencial na decisão clínica.
Os pacientes com diagnóstico de adenocarcinoma da próstata devem ser avaliados individualmente quanto à realização de exames para o estadiamento, dependendo da classificação de risco (valores de PSA, grau de ISUP, número de fragmentos positivos, estádio clínico), além das condições clínicas, idade e expectativa de vida do paciente, pois são fatores importantes na tomada de decisão.
Atualmente, sempre que possível, a decisão do tratamento em alguns casos deve ser multidisciplinar, incluindo o Radio-oncologista e o Oncologista clínico. Em pacientes de muito baixo risco, com expectativa de vida superior a 10 anos, deve ser oferecida sempre a vigilância ativa, informando-o e compartilhando a necessidade de reavaliação periódica, re-biópsias e probabilidade de mudança de conduta nos casos de alteração do grau tumoral, aumento da extensão ou progressão da doença.
A braquiterapia é uma opção naqueles pacientes de baixo risco, com maior volume de doença e que desejam tratamento, mas sempre observando os critérios como próstata < 40 gramas e ausência de sintomas miccionais obstrutivos.
Nos pacientes com risco intermediário e alguns casos selecionados de doença de alto risco a cirurgia é a primeira opção, conforme a maioria dos guidelines. A prostatectomia radical, incluindo a linfadenectomia estendida nos pacientes de risco para comprometimento linfonodal (baseada no nomograma de Briganti) pode ser realizada por via aberta (minilaparotomia infraumbilical), laparoscópica ou robótica assistida.
Dados recentes da literatura sugerem resultados funcionais e oncológicos semelhantes entre a cirurgia aberta com cirurgiões experientes e de grande volume e a prostatectomia robótica, sendo esta última via cada vez mais atraente aos pacientes, oferecendo menor tempo de hospitalização, menos sangramento, mas ainda com custos elevados e restrita a centros especializados e de alto volume.
REFERÊNCIAS BIBLIOGRÁFICAS
GUIDELINES ON PROSTATE CANCER, 2021- EAU https://uroweb.org/guideline/prostate-cancer/
CLINICALLY LOCALIZED PROSTATE CANCER: AUA/ASTRO /SUO GUIDELINE 2017
CÂNCER DE PROSTATA LOCALIZADO- PROJETO DIRETRIZES -AMB/SBU

1. Qual é o câncer mais comum em homens?
O carcinoma de pele não melanoma (desconsiderado em alguns casos por ser indolente) é o câncer mais comum em homens; o câncer de próstata é o segundo tipo de mais frequente.
2. Em quais países há maior incidência de câncer de próstata? A que essa incidência deve ser atribuída?
Países de maior nível socioeconômico, como Nova Zelândia, América do Norte e Austrália; países da Ásia apresentam incidência inferior.
Essa incidência pode ser atribuída ao maior acesso ao exame de antígeno prostático específico (PSA), à dieta (rica em gordura) e à menor exposição ao sol.
3. Em relação à mortalidade, quais países apresentam maiores índices? A que esses dados devem ser atribuídos?
Os países que apresentam os maiores índices de mortalidade por câncer de próstata são Caribe e África. Esse índice deve-se ao maior número de afrodescendentes.
4. Quais são os fatores de risco relacionados com o câncer de próstata?
• Obesidade: tumores de alto grau
• Síndrome metabólica
• História familiar: apenas 10% apresentam câncer hereditário
• Afrodescendentes: doença mais agressiva
• Dieta
• Álcool
• Gordura
• Tabagismo
• Testosterona (reposição em hipogonadismo); não está associada ao aumento de câncer de próstata.
5. Como é feito o rastreamento do câncer de próstata e qual a idade para iniciá-lo?
O rastreamento é feito por meio do exame digital associado ao PSA. Segundo a Sociedade Brasileira Urologia (SBU), ele deve ser iniciado aos 50 anos. Em caso de afrodescendentes ou paciente com história familiar, iniciá-lo a partir dos 45 anos.

6. Comente a respeito do valor de normalidade do PSA e o que pode estar associado a suas alterações?
O valor de referência de normalidade para PSA é de 2,5 ng/ml, porém, esse valor pode alterar à medida que o indivíduo envelhece. Como é um exame pouco específico, pode estar elevado em casos de prostatite, hiperplasia prostática benigna (HPB) e câncer de próstata.
7. Quando encaminhar o paciente para o urologista?
Quando o PSA for maior que 2 ng/ml. Pacientes com PSA menor podem ser acompanhados por generalistas, caso não seja indivíduo de risco (afrodescendentes ou com história familiar de câncer de próstata).
8. Além do PSA, quais outros testes podem ser utilizados para reduzir o número de pedidos de biópsia para câncer de próstata?
PSA livre/total; densidade de PSA; velocidade PSA; índice de saúde prostática; gene 3 do câncer de próstata (PCA3).
9. Quais as indicações para biópsia de próstata?
Calculadora de risco (que leva em conta exame físico e outros testes), PSA maior que 10 e presença de nódulo na próstata – por meio de testes adicionais comentados acima. O diagnóstico de câncer de próstata é confirmado somente por biópsia.
Quando o PSA está entre 2,5 e 10 ng/ml, deve-se repeti-lo e/ou continuar a investigação por meio de outros exames (principalmente PSA livre/total) e pela velocidade de aumento do PSA.
A ultrassonografia (USG) transretal é o método de escolha para a realização da biópsia prostática, cuja finalidade é orientar o posicionamento da agulha nas diferentes zonas da próstata.

10. Quais são os achados de biópsia de próstata?

11. O que é o escore de Gleason e qual sua importância?
O escore de Gleason corresponde ao padrão de diferenciação das células (morfologia, forma do núcleo e arquitetura). É umafferramenta importante para avaliar os estágios do adenocarcinoma de próstata, o que possibilita informar o prognóstico da doença a partir do grau de diferenciação encontrado.
12. Comente a respeito dos valores de Gleason e sua correspondência com o ISUP (Sociedade Internacional de Patologia Urológica).
O escore avalia qual é o primeiro e o segundo padrão de células mais comuns encontrados dentro do adenocarcinoma de próstata. O primeiro número somado indica o padrão predominante na biópsia, o que é um fator de melhor ou pior prognóstico.
Recentemente, foi criado o ISUP, um sistema formado a partir da classificação de Gleason, que facilita a avaliação de diferenciação do adenocarcinoma e a análise do seu prognóstico.
No quadro abaixo, é possível observar a correspondência entre os valores de ambas as classificações.

13. Discuta a respeito do estadiamento TNM do tumor de próstata e seu significado.
O TNM é um estadiamento padronizado que classifica o tumor conforme sua localização e disseminação por meio das estruturas próximas à próstata. É importante, pois permite que o médico discuta com o paciente sobre qual tratamento é mais adequado.


14. Como é feito o estadiamento do tumor?
Por meio de um conjunto de exames físicos, laboratoriais e de imagem.


15. Classifique o câncer de próstata em carcinoma de baixo risco, risco intermediário e alto risco conforme o PSA, a escala de Gleason e a extensão local.
A classificação de risco completa pode ser observada na tabela a seguir.
Na classificação de risco intermediário e alto risco, somente PSA ou Gleason ou extensão local (observada pela TC ou toque retal) são capazes de classificá-lo.
Em caso de tumor localmente avançado, o importante é observar a extensão local, independente do PSA ou do Gleason.

16. O que avaliar no tratamento do paciente?
• A agressividade do câncer
• O risco de disseminação
• A expectativa de vida conforme idade e comorbidades
17. Quais são os marcadores moleculares do câncer de próstata?
Marcadores moleculares
• DECIPHER
• PROLARIS
• ONCOTYPE
• PROMARK
18. Cite as vantagens e desvantagens relacionadas aos marcadores moleculares.
Vantagens
• Avalia a possibilidade de recidiva do câncer
• Avalia qual o melhor tratamento para o tipo de câncer (radioterapia o cirurgia)
• Informa a possibilidade do câncer ser mais agressivo ou menos agressivo
Desvantagens
• Relacionadas com o alto custo da utilização desses marcadores e, consequentemente, com a falta de acesso.
19. Comente a respeito dos tipos de tratamento de câncer de próstata, destacando os mais utilizados.

20. Relacione os tipos de tratamento mais comuns para câncer de próstata segundo a classificação de risco.

Observação: risco intermediário desfavorável corresponde ao padrão 4 + 3 de Gleason ou ISUP 3.
21. Descreva os critérios para a realização de vigilância ativa para um paciente com câncer de próstata?
• T1C
• Gleason 6
• PSA < 10 ng/ml, densidade do PSA < 15
• < 3 fragmentos positivos ou menos que 50% do fragmento acometido pelo câncer (doença de caráter indolente)
22. Em que consiste o tratamento baseado na vigilância ativa?
Repetir PSA e exame físico a cada seis meses; realizar uma nova biópsia em um ano (biópsia confirmatória).
Observação: a vigilância ativa permite que o paciente não realize um tratamento mais agressivo, caso não se confirme que o câncer evoluiu.
23. Quais são os fatores que induzem a mudança do tratamento?
• Mudança de Gleason
• Elevação do PSA
• Opção do paciente
24. Informe qual é o tratamento considerado padrão-ouro para câncer de próstata localizado.
A prostatectomia radical é considerada o tratamento padrão-ouro para o câncer de próstata localizado. Não há evidências de que outros tratamentos sejam mais eficazes no controle da doença e no desfecho de mortalidade.
25. Comente a respeito da prostatectomia radical, suas dificuldades e suas indicações.
• Indicações: pacientes com risco intermediário ou alto.
• Dificuldades: preservar feixes nervosos relacionados com as funções autonômicas.
• Efeitos colaterais: incontinência urinaria (3%-5%) após seis meses.
• Disfunção erétil (20%-30%): utilização de medicamentos orais (por exemplo: tadalafila), locais (por exemplo, prostaglandinas) ou próteses penianas.
• Margens positivas (16%-24%), que leva à recidiva da doença: hormonioterapia ou radioterapia.

26. Disserte sobre o que o patologista deve descrever ao avaliar o tecido neoplásico.
Prostatectomia radical
• Escore de Gleason
• Percentual do tumor/tamanho
• Margens cirúrgicas
• Número de linfonodos
27. Discuta a respeito da braquiterapia, comentando suas principais indicações.
A braquiterapia consiste na inserção de sementes de iodo radioativo na próstata. Para que haja resultados positivos, o adenocarcinoma deve ser localizado e de baixo grau, caso contrário sua realização não é indicada.
Deve-se lembrar que esses pacientes podem ser submetidos à prostectomia radical, que apresenta maiores índices de sucessos.
Critérios
• T1-T2
• Gleason 6
• PSA < 10 ng/ml
• Próstata com menos de 50 g
• International Prostate Symptom Score (IPSS) < 12
28. Disserte sobre a radioterapia externa e suas indicações.
A radioterapia externa é uma das opções de tratamento para o câncer de próstata clinicamente localizado; pode ser indicada para todos os três grupos prognósticos, isolada ou em associação com hormonioterapia, conforme o estadiamento. Como já mencionado, pode ser aplicada por meio de diversas técnicas.
Porém, necessita de aparelhos extremamente caros e indisponíveis na maior parte do país.
29. Como deve ser o cuidado após a cirurgia?
Pacientes devem ser acompanhados após seis meses de cirurgia para avaliar se houve recidiva ou não.
Caso haja uma elevação do PSA maior que 0,2 ng/ml, há a possibilidade de recidiva, seja por metástases seja por disseminação nos linfonodos.
Deve-se usar o PET-PSMA para localizar os possíveis sítios de recidivas e avaliar se eles são localizados ou sistêmicos.

30. Em caso de doença metastática, como deve ser a conduta?
O tratamento inicial é com bloqueio hormonal. Caso haja falha no tratamento, podem ser utilizados novos medicamentos, conforme o fluxograma abaixo.

Observação: alto custo e medicamentos recém-liberados.
Artigos relacionados ao tema
O Revisamed-Revisional em Medicina selecionou também outros artigos publicados em periódicos e revistas científicas que podem complementar os seus estudos na área de Câncer de Próstata.
Para ter acesso, basta clicar nos títulos abaixo:
São eles:
Classificação e terapia do câncer de próstata de alto risco
Estratégias de tratamento atuais para câncer de próstata avançado
Você pode gostar também do artigo: O tratamento cirúrgico do câncer de próstata
Gostou do artigo? Estes e outros temas você acompanha em nosso blog e no Portal Medicina Atual, o portal de conteúdo médico do Revisamed.